Неизвестный танк часть 3
- Опубликовано: 18.04.2016, 19:06
- Просмотров: 197988
Содержание материала
Неизвестный танк...
(Раздел создан на основании книги "Танк" Военного издательства Министерства Обороны СССР 1954 года, под редакцией
Антонова А.С., Артамонова Б.А., Коробкова Б.М., Магидович Е.И. и других материалах.)
Часть 3
ГЛАВА ШЕСТАЯ
БРОНЕВАЯ ЗАЩИТА
Броневая защита — одно из основных боевых свойств танка. Со времени появления танка его броневая защита непрерывно
совершенствовалась. Увеличивалась толщина брони, улучшались ее свойства, фоорма корпуса и башни танка изменялась так, чтобы повысить их стойкость против снаряда. Все это было вызвано развитием и совершенствованием средств противотанковой борьбы, прежде всего противотанковой артиллерии.
Поэтому, рассматривая свойства брони и броневую защиту танка мы должны будем в эгой главе уделть внимание средствам борьбы против танков и рассмотреть действие этих средств, в первую очередь бронебойных снарядов, на броню.
БРОНЯ
СВОЙСТВА БРОНИ
Танковая броня изготовляется исключительно из специальной (ле гированиой) стали. Это объясняется тем, что при сравнительно небольшой толщине только такая сталь удовлетворяет сложным требованиям, предъявляемым к броне.
Броня должна противостоять огромным ударным нагрузкам. Так, например, 76-мм бронебойный снаряд обладает запасом энергии, которой хватило бы, чтобы поднять десятитонную машину на высоту шести этажного дома. При ударе о броню эта энертия расходуется почти мгно венно, вследствие чего развивается громадная мощность— для 76-мм снаряда до 800 000 л. с. Броня должна отразить или поглотить эту энергию (при прямом попадании), не давая сквозного поражения.
Какими же основными свойствами должна обладать броня, чтобы оказаться стойкой против снаряда?
Попробуем выяснить это на простых примерах.
Медную пятикопеечную монету можно сравнительно легко проколоть иголкой. Для этого иголку нужно вставить в пробку, чтобы она не прогибалась при ударе, поставить пробку на монету и ударить по иголке молотком. Но та же иголка сломается или затупится, если пытаться проколоть ею чугунную пластинку. При ударе же молотком медная монета сплющится, а чугунная пластинка от такого удара расколется.
Подобно игле, прокалывающей монету, снаряд, калибр которого невелик по сравнению с толщиной брони, может только проколоть ее. Чем тверже в этом случае броня, тем лучше она противостоит проколу. Снаряд большого калибра проломит хрупкую броню или отколет куски металла с тыльной стороны ее, в то время как в вязкой броне образуются лишь выбоины или вмятины — вязкий материал поглотит энергию сна ряда полностью, не давая пробоины.
Значит, броня должна быть одновременно итвердой и вязкой (не хрупкой). К сожалению, эти два свойства противоречивы: вязкий металл обычно недостаточно тверд, твердый — обычно хрупок. Можно лишь несколько повысить твердость при данной вязкости или, наоборот, при данной твердости немного увеличить вязкость.
СТРОЕНИЕ СТАЛИ
Более или менее удовлетаорительное сочетание твердости и вяэкостн стали обеспечивается ее составом и термической (тепловой) обработкой, Броневая сталь является разновидностью специальной (легировааной) конструкционной стали, т. е. стали, предназначенной для изготовления деталей различных машин и механизмов. Такое совпадение не является случайным, так как возможно лучшее сочетание твердости и вязкости обязательно и для деталей машин.
Сталь — это сплав железа с углеродом. Несколько десятых долей процента углерода, добавляемые к железу, превращают этот сравнительно мягкий и весьма пластичный, тягучий металл в сплав, которому последующая термическая обработка позволяет придать самые разнообразные свойства: сталь одного и того же состава может быть сделана чрезвычайно твердой и хрупкой, но может приобрести и большую вязкость при значительном (по сравнению с железом) увеличении твердости.
Чтобы понять причины этого, рассмотрим явления, которые происходят в стали при ее нагреве и охлаждении.
Когда сталь расплавлена, в ней нельзя различить частицы железа и углерода, как в соляном растворе неразличимы вода и соль. Мельчайшие частицы обоих веществ, в данном случае молекулы воды и соли, настолько тесно связаны между собой, что их нельзя разделить механическим способом, например отстаиванием или процеживанием. В этом отношении раствор резко отличается от смеси, какую представляют собой, например, взболтанная в воде глина или смешанное с водой масло.
Раствором является жидкая сталь. В железе, как в воде соль, растворен углерод и другие примеси, попадающие в сталь из сырья и топлива (например, сера, фосфор) или специально добавляемые при изготовлении стали для улучшения ее свойств (например, кремний, марганец).
Если охлаждать расплавленную сталь, то при определенной температуре (примерно между 1400 и 1535°Ц, в зависимости от содержания углерода) она застывает и кристаллизуется.
Процесс застывания стали и ее кристаллизация заключаются в том, что атомы железа, расположенные в жидком металле без всякого порядка, «выстраиваются» и образуют так называемую кристаллическую решетку, состоящую из огромного количества одинаковых элементарных ячеек. Элементарные ячейки представляют собой, подобно сотам, одинаковые «по форме и размерам и тесно примыкающие одна к другой простые геометрические фигуры. Так, атомы железа в застывшей стали образуют фигуры гранецентрированного куба (рис. 301).
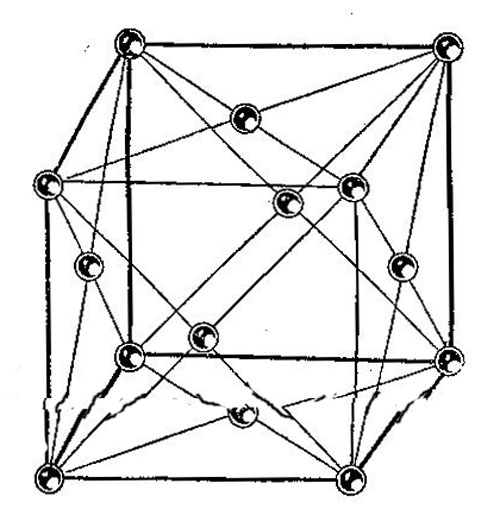
Рис.301. Схема ячейки гранецентрированного куба
Каждая элементарная ячейка сложена из четырнадцати атомов — восемь в вершинах граней и по одному в центре каждой из шести граней куба. Эти ячейки настолько малы (на длине одного миллиметра их можно разместить свыше двух миллионов), что неразличимы даже в самые сильные современные микроскопы, в том числе и электронные. Лишь специальным методом исследования при помощи рентгеновских лучей можно определить их форму и размеры.
Кристаллизация начинается одновременно во многих точках застывающего металла, В результате ее образуетсямножество небольших кристаллов, имеющих неправильную форму вследствие столкновения растущих кристаллов друг с другом. Такие неправильные (неполногранн ные) кристаллы называются зернами. Зерна в металле хорошо различаются под микроскопом (рис, 302) после специальной обработки — шлифовки и травления (обычно в слабом растворе кислоты).
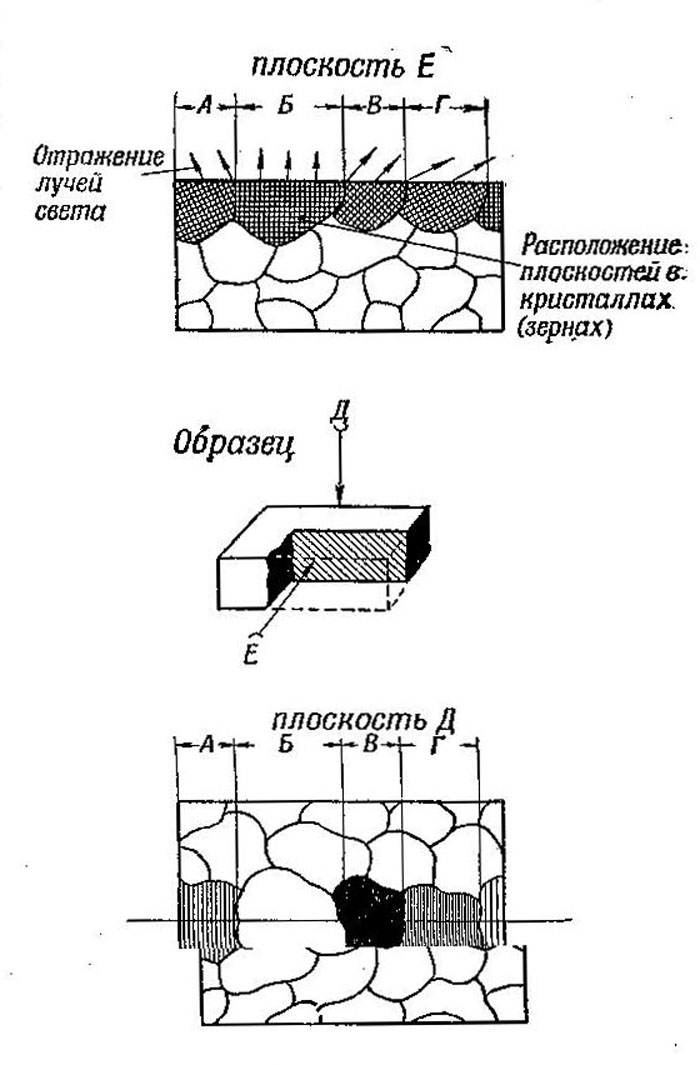
Рис. 302. Причина неоднородности свойств отдельных зерен металла
Травление действует на зерна неодинаково, и потому они поразному отражают падающий на них свет, как условно показано на рис. 302; вследствие этого под микроскопом отдельные зерна кажутся освещенными неодинаково — одни светлее, другие темнее.
Прочность кристаллов в различных направлениях неодинакова. Если бывсе кристаллы были расположены одинаково, то металл обладал бы различной прочностью в различных направлениях. Наличие же в куске металла не одного, а десятков и сотен тысяч кристаллов, плоскости которых наравлены различно, делает свойства литого металла одинаковыми во всех направлениях. Ясно, насколько это существенно для работы детали. Если такое условие не соблюдено и свойства металла в равличных направлениях почему-либо оказываются не одинаковыми, то это приходится учитывать при изготовлении детали.
Итак, первое превращение, происходящее при застывании расплавленной стали, заключается в ее кристаллизации: образуются зерна, представляющие собой кристаллы железа с гранецентрированной решеткой. Что же происходит при кристаллизации с углеродом, растворенным в жидкой стали?
Внутри кубика, образуемого атомами железа, есть свободное место. Атом углерода, величина которого меньше величины атома железа, может занять это место. Тесная связь между атомами обоих веществ сохранится: углерод окажется растворенным в твердом железе, как он был растворен в жидком. Его нельзя будет не только отделить от железа механическими способами, но и обнаружить под микроскопом. Только рентгеновские лучи покажут, что среди атомов железа вкраплены атомы углерода, которые также занимают строго определенные, хотя и не всесвободные места. Такой твердый раствор углерода в железе (имеющем гранецентрированную кристаллическую решетку) называется аустенитом, . Однако превращения в стали на этом не заканчиваются.
Дело в том, что форма кристаллической решетки большинства металлов при остывании не меняется, но немногие из них, в том числе железо, представляют исключение из этого правила. Атомы железа при охлаждении перегруппировываются, образуя новую фигуру — объемно-центрированный куб, сложенный из девяти атомов в каждой ячейке (рис, 303).
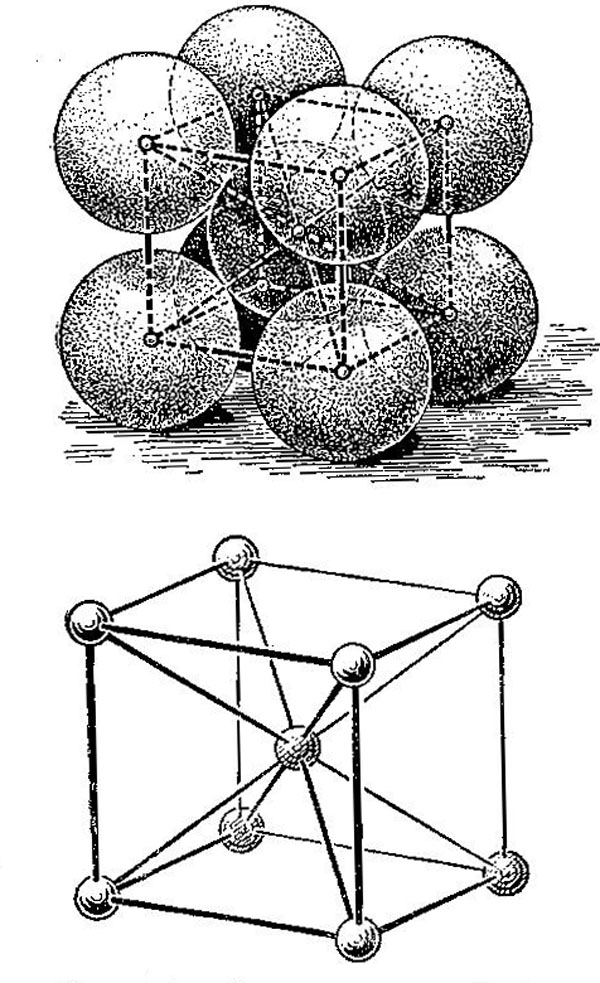
Рис. 303. Схема ячейки объемноцентрированного куба
В сталях в зависимости от их состава это превращение при весьма медленном охлаждении начинается при различных температурах (от 910° и ниже), но заканчивается всегда при одной и той же температуре (723° Ц).
В новой элементарной ячейке для атома углерода уже нет места; поэтому, углерод выходит из раствора* и образует с железом химическое соединение, называемое цементитом который обладает весьма большой твердостью ихрупкостью.
* В действительности в ненагретом железе углерод растворяется, но в ничтожном количестве, менее 0,01%. На практике этим пренебрегают.
В конструкционных сталях содержится не более 8—10% цементита, что может лишь сравнительно не намного увеличить их твердость.
Следует отметить разницу между твердым раствором и химическим соединением. В химическом соединении группировка атомов (кристаллическая решетка) совершенно другая, чем в составляющих его веществах, в то время как твердый раствор сохраняет группировку атомов растворителя (в данном случае железа). Особой формой кристаллической решетки химического соединения объясняется резкое отличие его свойств от свойств образующих его веществ.
Под влиянием особенностей превращения стали при ее охлаждении, на которых мы здесь не останавливаемся, цементит будет находиться не во всех зернах стали: часть их будет представлять почти чистое железо (феррит), часть — смесь феррита и цементита в виде чередующихся тонких пластинок (рис. 304, вверху). Такая смесь называется пластинчатым перлитом.
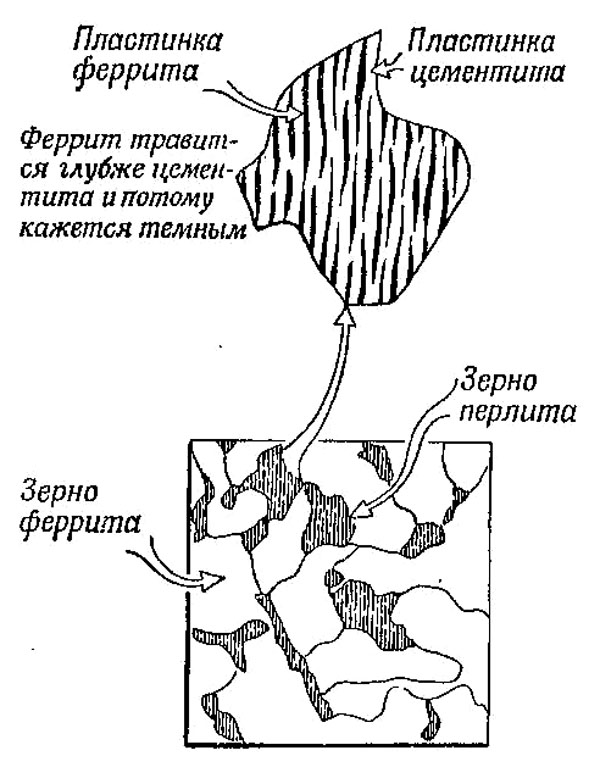
Рис.304. Микроструктура отожженной стали, содержащей 0,3% углерода

